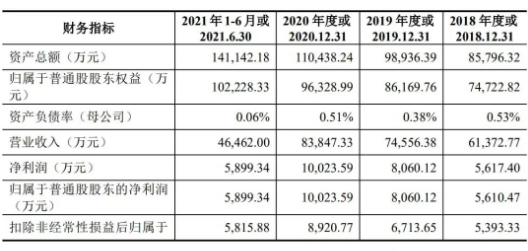
上交所近日发布实施《科创板发行上市审核规则适用指引第7号——医疗器械企业适用第五套上市标准》(简称《指引》),将科创板第五套上市标准的适用企业范围从创新药企业拓宽至医疗器械企业。

科创板第五套上市标准增强了对“硬科技”企业的包容性,支持处于研发阶段、尚未形成一定收入的企业登陆资本市场。开板以来,已有一批创新药研发企业采用该上市标准在科创板成功上市,初步形成了药品研发企业的集聚效应和示范效应。
《指引》在前期审核实践基础上,结合医疗器械领域科技创新发展情况、行业监管要求,对申请适用科创板第五套上市标准的医疗器械企业,从核心技术产品范围、阶段性成果、市场空间、技术优势、持续经营能力、信息披露等方面作出了细化规定。
一是细化核心技术产品范围。申请企业的核心技术产品应当属于国家医疗器械科技创新战略和相关产业政策鼓励支持的范畴,主要包括先进的检验检测、诊断、治疗、监护、生命支持、中医诊疗、植入介入、健康康复设备产品及其关键零部件、元器件、配套件和基础材料等。
二是明确取得阶段性成果的具体要求。申请企业应当至少有一项核心技术产品已按照医疗器械相关法律法规要求完成产品检验和临床评价且结果满足要求,或已满足申报医疗器械注册的其他要求。
三是关注市场空间的论证情况。申请企业的主要业务或产品,需满足市场空间大的要求,并应当结合核心技术产品的创新性及研发进度、临床需求和市场格局等,审慎预测并披露满足标准的具体情况。
四是要求具备明显的技术优势。申请企业需具备明显的技术优势,应当结合核心技术与核心产品的对应关系、核心技术先进性衡量指标、团队背景和研发成果、技术储备和持续研发能力等方面,披露是否具备明显的技术优势。
五是提出信息披露及核查要求。申请企业应当客观、准确披露核心技术产品及其先进性、研发进展及其阶段性成果、审批注册情况、预计市场空间、未来生产销售的商业化安排等信息,并充分揭示相关风险。(记者 钟国斌)



 TM奥义前瞻:黄金走出“过山车”后进入多头行情了吗?">
TM奥义前瞻:黄金走出“过山车”后进入多头行情了吗?">